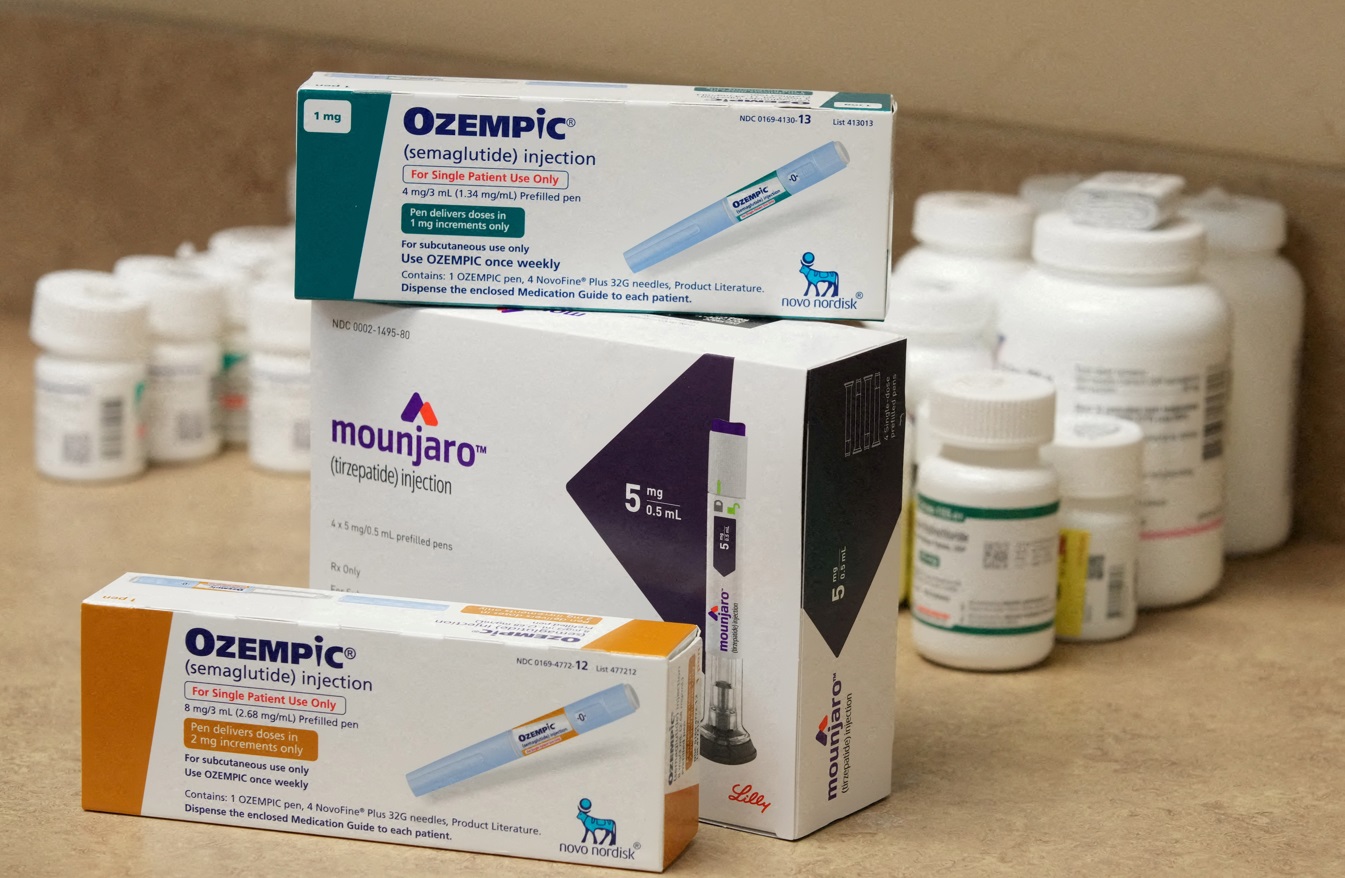
A expiração da patente do Ozempic, medicamento amplamente conhecido por seu papel no tratamento do diabetes tipo 2 e, off-label, na gestão da obesidade, gerou grande expectativa no mercado e entre os consumidores brasileiros. Muitos esperavam que o vencimento da exclusividade de produção, ocorrido em uma sexta-feira recente, abrisse caminho imediato para a entrada de novas versões e, consequentemente, uma significativa redução nos preços. Contudo, essa previsão ainda não se concretizou. O cenário atual revela que a jornada para a democratização do acesso ao Ozempic é mais complexa do que se imaginava, envolvendo uma série de etapas regulatórias e técnicas que estão em andamento. A chegada de medicamentos alternativos, como o próprio Ozempic, depende de um rigoroso processo de aprovação, especialmente por se tratar de uma substância de alta complexidade molecular, a semaglutida.
O intrincado caminho regulatório para novas versões
A Agência Nacional de Vigilância Sanitária (Anvisa) é o principal portal para a entrada de novos medicamentos no mercado brasileiro. Atualmente, a agência tem sob sua análise pelo menos 15 pedidos relacionados à semaglutida, em diferentes estágios de avaliação. Esse volume demonstra o interesse da indústria farmacêutica em explorar a lacuna deixada pela expiração da patente, mas também sublinha a complexidade do processo.
Parte considerável desses processos encontra-se na fase de “exigências técnicas”. Isso significa que a Anvisa solicitou informações adicionais às empresas proponentes, um passo comum e crucial para garantir a segurança e eficácia dos futuros produtos. As solicitações podem variar desde a necessidade de esclarecimentos sobre estudos clínicos apresentados até ajustes em métodos de análise e controle de qualidade. A Anvisa enfatiza que, no caso de medicamentos complexos, como os derivados da semaglutida, “é necessário um exercício de comparabilidade que comprove qualidade, segurança e eficácia compatíveis com o medicamento de referência”. Este critério é fundamental e reflete a natureza intrínseca da substância e a forma como é desenvolvida e avaliada globalmente.
A complexidade da semaglutida: um peptídeo e seus desafios
A semaglutida é uma substância ativa utilizada no tratamento do diabetes tipo 2 e da obesidade. Seu mecanismo de ação envolve o controle da glicose no sangue e a regulação do apetite, contribuindo para o manejo da doença e a perda de peso. Tecnicamente, a semaglutida é um peptídeo, uma molécula consideravelmente mais complexa do que os compostos químicos tradicionais que formam a base da maioria dos medicamentos genéricos. Sua produção é sofisticada e pode seguir diferentes métodos, o que impacta diretamente a forma como novas versões chegam ao mercado.
Ao contrário de medicamentos de estrutura simples, que podem ser reproduzidos como genéricos idênticos após a queda de patente, a semaglutida não permite cópias exatas. Em vez de genéricos, surgem biossimilares ou, em alguns casos, novos medicamentos que utilizam a mesma substância ativa. Para serem aprovados, esses produtos precisam comprovar, por meio de estudos próprios e detalhados, que sua qualidade, segurança e eficácia são comparáveis às do produto original. Entre os pedidos em análise na Anvisa, há abordagens distintas, incluindo versões sintéticas e biológicas do peptídeo. Farmacêuticas como EMS, Ávida Care e Cristália estão entre as empresas com projetos mais avançados nesse pipeline regulatório.
Barreiras técnicas e científicas na avaliação
A avaliação da Anvisa para medicamentos baseados em peptídeos como a semaglutida vai além da simples análise de composição. A agência escrutina aspectos cruciais como a resposta imunológica que o medicamento pode provocar no paciente, o controle rigoroso de impurezas presentes na formulação e a capacidade de identificar pequenas variações na estrutura molecular do peptídeo. Esse tipo de análise é inerentemente mais demorado e complexo do que o processo para medicamentos tradicionais, refletindo a natureza da própria substância.
Agências reguladoras em outros países seguem padrões de avaliação igualmente rigorosos para peptídeos. Para esses compostos, não basta apenas replicar a composição química; é imprescindível demonstrar que o produto se comporta de maneira equivalente no organismo humano, sem diferenças significativas que possam afetar a segurança ou a eficácia. A validação desses aspectos exige um alto nível de expertise técnica e científica.
Exigências específicas: da estrutura molecular à resposta no organismo
A análise de impurezas é um ponto crítico. Ela abrange desde resíduos do processo de fabricação, como solventes e metais pesados, até subprodutos que podem se formar durante a produção ou o armazenamento do medicamento. Mesmo em quantidades mínimas, essas substâncias podem ter impactos significativos na segurança do paciente ou na estabilidade do medicamento ao longo do tempo. As empresas devem demonstrar controle absoluto sobre essas impurezas.
As variações na molécula são outro aspecto sensível. Dado que a semaglutida é um peptídeo, pequenas alterações em sua estrutura, que podem ocorrer dependendo do método de produção empregado, têm o potencial de alterar a eficácia ou a duração da ação do medicamento no corpo. É responsabilidade das farmacêuticas comprovar que são capazes de identificar e controlar essas variações, assegurando a consistência e a padronização entre os diferentes lotes de produção. Esse controle de qualidade é vital para garantir que cada dose entregue ao consumidor seja exatamente como a de referência. Muitos dos pedidos em análise na Anvisa ainda aguardam uma avaliação inicial, o que sugere que a liberação de novas versões será um processo escalonado, dependendo do avanço individual de cada processo dentro da agência.
Preço e acessibilidade: um cenário distinto dos genéricos
Embora a expectativa de queda nos preços seja compreensível, é fundamental entender que a dinâmica para a semaglutida será diferente daquela observada com medicamentos genéricos comuns. Como explicado, a semaglutida não terá versões genéricas idênticas devido à sua complexidade molecular. As alternativas que chegarão ao mercado serão, em sua maioria, biossimilares ou novos medicamentos que utilizam o mesmo princípio ativo.
Em medicamentos tradicionais, a entrada de genéricos costuma gerar uma redução de preços de 35% ou mais, conforme dados históricos da Anvisa. No caso de biossimilares, essa redução tende a ser mais modesta, geralmente em torno de 20%. Isso se deve aos custos mais elevados de pesquisa, desenvolvimento e produção, bem como aos estudos de comparabilidade que precisam ser realizados. Adicionalmente, nem todos os pedidos em análise no Brasil seguem o caminho de biossimilaridade. Alguns foram apresentados como medicamentos novos, o que significa que não há, por definição, um compromisso direto com a redução de preço em relação ao produto original.
O impacto no bolso do consumidor: o que esperar
O impacto real no bolso do consumidor brasileiro continua condicionado ao avanço desses processos regulatórios e ao tipo de produto que, de fato, será aprovado e chegará às farmácias. Enquanto os pedidos seguem em análise na Anvisa, a oferta permanece limitada e os preços, elevados. A entrada gradual de biossimilares e, potencialmente, de novos medicamentos, poderá trazer alguma concorrência e, consequentemente, uma pressão para a redução dos custos. No entanto, é improvável que se observe uma queda brusca e acentuada como a que ocorre com os genéricos de medicamentos de pequenas moléculas.
A perspectiva de maior acessibilidade ao Ozempic e seus análogos dependerá da celeridade e da conclusão bem-sucedida das avaliações da Anvisa, bem como das estratégias comerciais das farmacêuticas que conseguirão a aprovação. É um processo que demanda tempo, rigor científico e transparência para assegurar que os novos produtos ofereçam a mesma qualidade e segurança que os pacientes esperam.
Perguntas frequentes
1. Por que a queda da patente do Ozempic não resultou em genéricos mais baratos imediatamente?
A semaglutida, princípio ativo do Ozempic, é um peptídeo, uma molécula complexa que não pode ser copiada exatamente como um genérico tradicional. As novas versões precisam passar por rigorosos estudos de comparabilidade para serem aprovadas como biossimilares ou novos medicamentos, o que demanda tempo e processos regulatórios extensos na Anvisa.
2. O que são biossimilares e como eles se diferenciam dos genéricos?
Biossimilares são medicamentos biológicos que são altamente semelhantes a um produto biológico de referência já aprovado. Diferente dos genéricos (que são cópias exatas de medicamentos químicos), os biossimilares são produzidos em organismos vivos e não podem ser idênticos, mas devem demonstrar comparabilidade em qualidade, segurança e eficácia.
3. Qual a expectativa de redução de preço para o Ozempic com a chegada de novas versões?
A expectativa é de uma redução de preço mais gradual e menos acentuada do que a dos genéricos. Enquanto genéricos podem reduzir preços em mais de 35%, biossimilares tendem a ter quedas em torno de 20%. Além disso, alguns pedidos na Anvisa são para novos medicamentos, sem compromisso direto com redução de preço em relação ao original.
Mantenha-se informado sobre os avanços regulatórios e as novas opções de tratamento para tomar as melhores decisões de saúde.
Fonte: https://www.infomoney.com.br